一、血制品行业发展规模
血液制品主要指以健康人血浆为原料、采用生物学工艺或分离纯化技术制备的生物活性制剂。血液制品在某些特定疾病的治疗上发挥着重要作用。
全球血制品行业呈现寡头竞争的格局,七大厂商2015年血制品营收合计149.08亿元,占全球市场的78.84%;其中,Grifols、Baxalta及CSL三巨头2015年血制品的营收都在30亿美元以上,和第四名Octapharma的17亿美元有着明显的距离。
全球血制品市场(不含重组)消费结构中,免疫球蛋白在血制品市场占比51%,白蛋白和血源凝血因子分别占15%和18%的份额。其中,在免疫球蛋白市场上,CSL、Baxalta和Grifols平分秋色;CSL在白蛋白市场上处于领先位置;Grifols在血源凝血因子、A1PI和特免细分市场上占比居首位。
全球血液制品市场构成情况
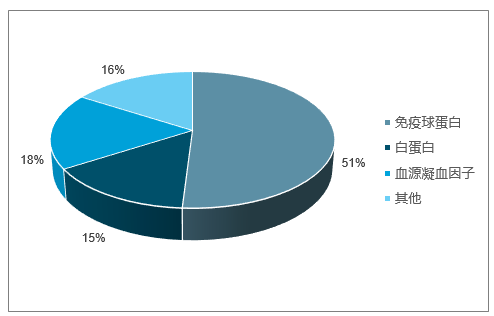
数据来源:公开资料整理
我国血液制品生产始于上世纪60年代,从两三家生产企业,发展到上世纪90年代,血液制品生产企业总数增加到70家左右。近年来,随着监管部门推动生产工艺升级,大部分小型生产企业被淘汰。根据中国食品药品检定研究院发布的《2017年生物制品批签发年报》,2017年全国共有29家境内血液制品生产企业申请批签发。
近年来,随着我国推动药品生产工艺升级,血液制品企业间兼并、整合加速,血液制品行业的集中度加强。有数据显示,2017年国内血液制品企业合计采浆量为8000多吨,华兰生物、上海莱士、泰邦生物、天坛生物的控股股东中国生物的采浆量总和占全国采浆量近60%。天坛生物、上海莱士和华兰生物等企业年采浆量均超过千吨,我国血液制品行业形成多强并立的局面。
根据批签发数量及平均中标价测算,中国2017年血液制品(不包含重组)市场规模约为274亿元。2017年版国家基本医疗保险、工伤保险和生育保险药品目录中,共有8个血液制品进入医保目录,其中新增品种4个。品种的增加和报销范围叠加,都会相应增加相关血液制品的需求,刺激血液制品行业再次提速。预计2018年血液制品市场规模将逼近300亿元。
2012-2018年中国血液制品市场规模走势
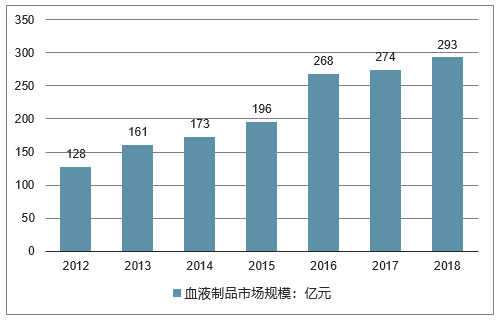
数据来源:公开资料整理
1、 我国的采浆规模情况分析
我国采浆量在经历了 2016 年的快速增长后增速回落,凝血因子类、免疫球蛋白类产品份额不断上升。
我国采浆规模正在不断增长。目前我国的采浆规模约为 8800吨。2008-2018 年,我国采浆规模增长了 1.8 倍,CAGR 约 11%。我国采浆规模受政策影响较大。在过去的 20 年里,我国政府对血制品行业的管制逐渐规范。1996 年,国务院颁布《血液制品管理条例》,标志着中国血液制品管理进入法制化轨道。1998 年,血液制品实行 GMP 准入制度。2001 年,国家规定不再批准新的血液制品生产企业。2004-2008 年,行业严格管理进一步深化,国家分别开启了批签发制度、检疫期制度,并进行了单采血浆改制。2011 年,贵州省卫生厅共关停了 16 家浆站,导致全国采浆量降低。2012 年卫生部提出血液制品倍增计划,希望能够增加血液供应。
2015 年,血液制品价格放开,血浆站的新建加速,采浆量规模随之快速增长。
我国历史采浆量变化

数据来源:公开资料整理
我国的血浆供给水平远低于美国等发达国家。根据估算,2018 年我国的采浆量约为 8800 吨,目前我国人口数约为 13.9 亿人,人均采浆量约为 6.4mL。而美国 2015 年采浆量为 3.11 万吨,人口数量为 3.2 亿人,人均采浆量为 97.2mL。我国人均采浆量仅为美国的 1/15。
美国和中国平均每人生产用血浆供给水平(mL)
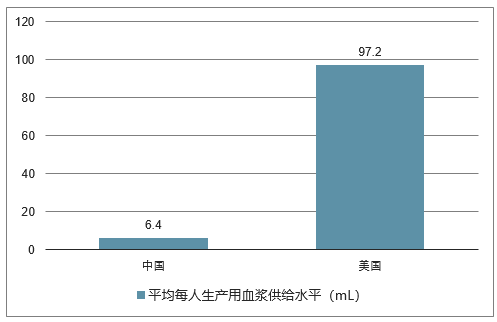
数据来源:公开资料整理
我国政府对血制品行业的监管较为严格,在一定程度上限制了采浆量的快速增长。一方面,我国的血浆来源只有单采血浆,回收血浆不允许用于血制品的生产,对比美国有 20%的血浆来自回收血浆,日本有 50%的血浆来自回收血浆。另一方面,我国政府限制企业进入血制品行业,2001 年,国家规定不再批准新的血液制品生产企业。目前我国血制品企业仅有 28 家,其中规律生产的企业约 20家,未来随着行业并购的增加,血制品企业数量可能会继续减少。此外,我国对单采血浆站的审批程序较为复杂,要求也比较严格。血液制品生产企业设置单采血浆站要符合当地单采血浆站设置规划,并且既要获得当地的县、市卫生局同意,又要有省级人民政府卫生行政部门的批复。而且,单采血浆站不得与一般血站设置在同一县行政区划内受十三五规划的影响,预计我国采浆量在未来两年将继续保持放缓的增速。
我国浆站的审批速度在经历了 2016 年的快速增长后,2017 年和 2018 年明显回落,预计这种审批速度放缓的状态在未来 2 年内将会持续。在 2016 年卫计委 66 号文《关于促进单采血浆站健康发展的意见》中,国家卫计委和 CFDA 提出要严格新增单采血浆站设置审批。根据对各省市的十三五单采浆站设置规划的整理,很多人口大省,也是主要供应血浆的省份,到 2020 年(十三五规划期末)剩余可批的单采血浆站的名额已经不多。
我国历年新增单采血浆站的数量
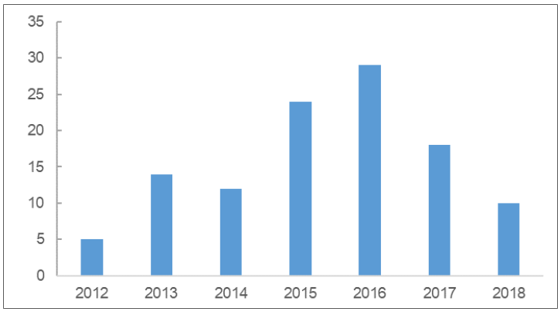
数据来源:公开资料整理
分品种来看,凝血因子类产品市场份额快速上升,白蛋白市场份额逐年下降,免疫球蛋白类产品市场份额比较稳定。目前白蛋白占据我国血制品行业最大的市场份额,根据样本医院的数据,2018 年前三季度我国血制品销售额中,白蛋白的市场份额最高,为 51%。但从 2012 年至今的趋势来看,白蛋白的市场份额从2012 年的 61%下降到 2018 年 Q1-3 的 51%。而凝血因子类产品(包括了图 15中的人纤维蛋白原、凝血因子和凝血酶及美元混合物)的市场份额逐步提升,从2012 年的 9%提高到 2018 年 Q1-3 的 18%。免疫球蛋白类产品的市场份额较为稳定,2012 年至今保持在 30%左右。
我国样本医院血液制品各品种市场份额
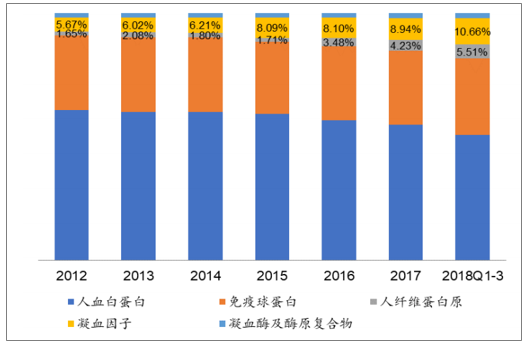
数据来源:公开资料整理
2、 我国血制品行业逐渐进入去库存的尾声,明年有望恢复健康增长
2017 年底,我国血制品生产商和经销商的的库存都达到了高位,主要原因有:
(1)随着 2015 年以来,单采血浆站审批速度的加快,我国血浆供给量增长加速,生产端血制品供给量增速提高;(2)2017 年医药流通行业改革,两票制的实施一方面使得很多小经销商无法存活,大经销商无法再通过这些小经销商进行销售,需要自己增加渠道铺设,一方面,经销商整合之后话语权增大,以前经销商小而散的时候,存货更多从生产商向经销商倾斜,而经销商话语权变大之后,经销商存货的意愿降低;(3)药占比、医保控费等政策的实施对销售额较大的人血白蛋白的终端需求有一定影响。经过一年多的渠道改革之后,渠道销售逐渐恢复,生产商和经销商都进入了去库存的阶段
经销商端-兴科蓉(剔除了2016年收购的影响)库存情况
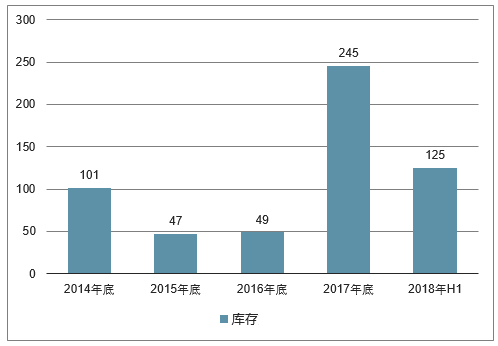
数据来源:公开资料整理
生产商端-华兰生物(这里只统计了库存商品的变化,不包括在产品、原材料等)库存情况
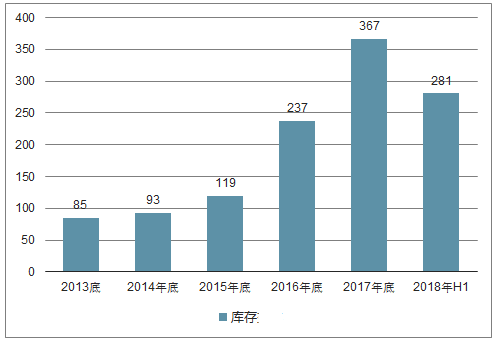
数据来源:公开资料整理
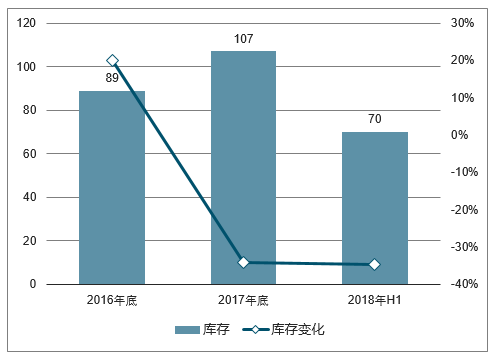
博雅生物库存情况
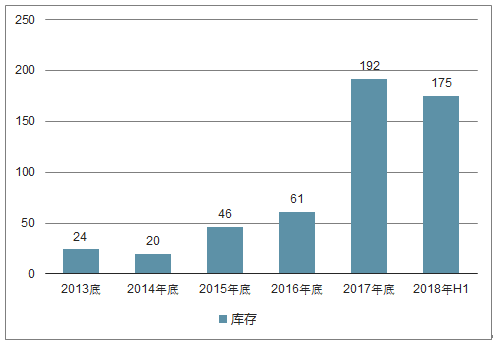
数据来源:公开资料整理
振兴生物库存情况
数据来源:公开资料整理
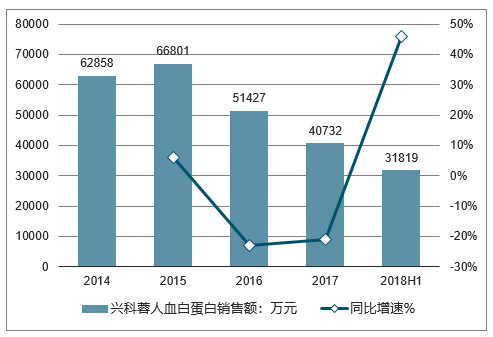
从进口人血白蛋白 Octapharm 的经销商兴科蓉的销售情况来看,经销商已逐渐从两票制的影响中恢复,销量回升。血制品生产厂商销量增速的恢复要慢于经销商,因为经销商在理顺渠道恢复正常销售之后,要先去除之前由于两票制而形成的高库存之后,才会增加进货量(不包括血制品生产厂商直销的情形。
兴科蓉人血白蛋白销售额变化
数据来源:公开资料整理
二、血制品行业市场需求情况分析
1、 纤原临床需求大
人纤维蛋白原主要用于治疗先天性或获得性纤维蛋白原缺乏症、弥散性血管内凝血;产后大出血和因大手术、外伤或内出血等引起的纤维蛋白原缺乏而造成的凝血障碍。属于凝血因子类。纤原属于创伤急救药,由于纤原是体内凝血机制的最后一个环节,临床止血效果最好。
人纤维蛋白原在生产工艺上,不同企业之间存在差别,造成吨浆产量、溶解时间的差别较大。先进的产品制备方法和工艺控制水平使公司具有良好的收得率,公司采用低温乙醇法结合层析工艺生产静注人免疫球蛋白,在保证质量的前提下,较单纯的低温乙醇法具有更高的收得率。
我国纤原市场仍有巨大的临床需求未被满足。剖宫产是纤原在临床应用的主要场景之一,我国与德国的剖宫产率相近,但是我国的人均纤原用量仅为德国人均纤原用量的 1/7。我国纤原市场的需求远未得到满足。
中国与德国纤原使用情况对比

数据来源:公开资料整理
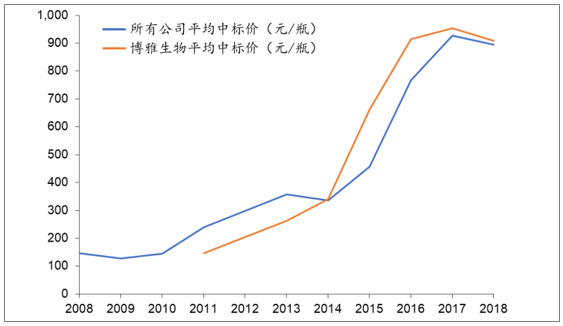
纤原价格在 2015 年发改委放开价格管制后上涨了近 1 倍,近 2 年受两票制和渠道库存增加的影响,价格略有下滑。2015 年,发改委放开对血制品的价格管制。作为临床紧缺的药物,纤原从 2015 年开始大幅提价。随后 2016 年,厂家开始大幅扩产,造成渠道库存增加。再加上 2017 年两票制的影响,最终导致 2017年我国纤原批签发量有所下滑,价格也在去库存的压力下略有下降。2018 年,我国纤原批签发量同比减少主要由于上海莱士批签发量大幅减少。
人纤维蛋白原中标价格变化
数据来源:公开资料整理
我国人纤维蛋白原历年批签发量变化

数据来源:公开资料整理
博雅生物人纤维蛋白原历年批签发量变化
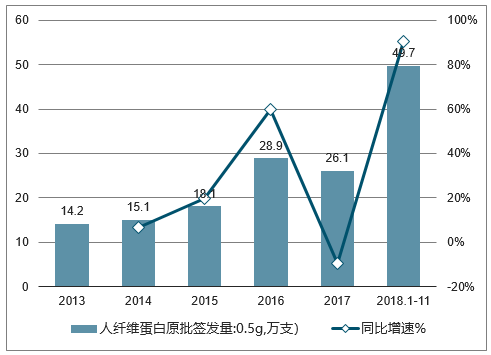
数据来源:公开资料整理
2、 白蛋白市场份额情况分析
白蛋白是我国唯一一个允许进口的血制品,供给不受国内采浆量的限制,进口企业参与竞争。根据我国的历年的批签发量来看,进口企业供应白蛋白的占比在50%~60%之间。
人血白蛋白进口与国产市场份额变化
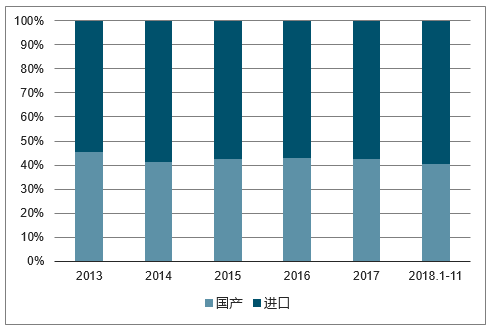
数据来源:公开资料整理
中国人均白蛋白用量已经达到部分发达国家的水平。据统计,2016 年我国人均白蛋白用量为 284g/千人口,虽然与美国相比,仍只有为美国人均白蛋白用量的一半,但已经达到德国、意大利、葡萄牙等发到国家水平。
中国和其他国家白蛋白用量水平比较(g/千人口)
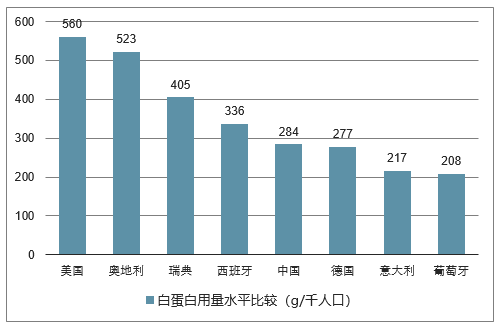
数据来源:公开资料整理
我国人血白蛋白批签发量保持 10-20%的增长。2017 年受两票制影响,我国白蛋白批签发量同比增速下降,2018 年我国白蛋白的批签发量同比增速恢复到10-20%的区间。近两年,我国国产白蛋白的批签发量同比增速略低于整体同比增速。白蛋白在我国医生和患者中的认可度较高,在控制药占比、处方外流的政策背景下,白蛋白院内市场增速放缓,但院外市场正在快速增长。
我国人血白蛋白批签发量年度变化
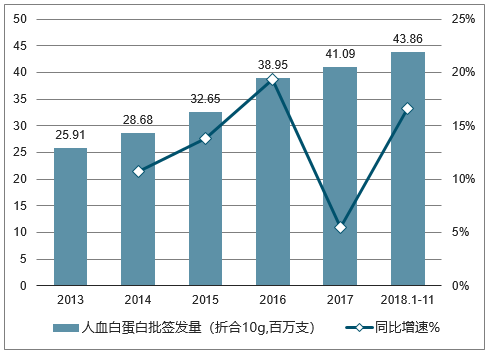
数据来源:公开资料整理
国产人血白蛋白批签发量年度变化
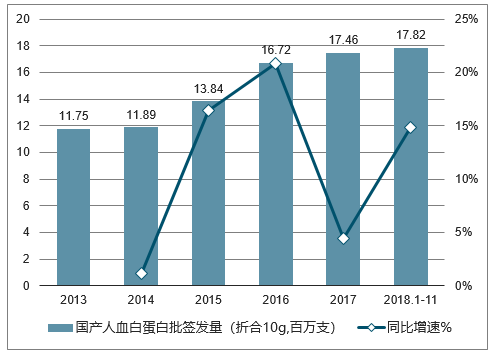
数据来源:公开资料整理
我国白蛋白价格相对稳定。从历年我国白蛋白平均中标价格来看,自 2008 年以来,我国白蛋白平均中标价在 350-450 元(10g/瓶)之间波动。
我国白蛋白每年平均中标价格变化(10g/瓶)
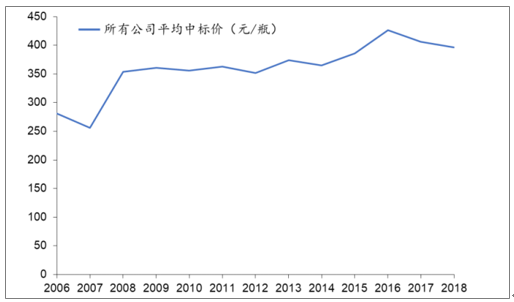
数据来源:公开资料整理
我国人血白蛋白市场竞争激烈,进口企业和国产企业加起来超过 20 家。从 2018年的批签发情况来看,市场份额最高的为外资企业 CSL。同时也可以发现,国产企业白蛋白的市场份额与采浆量相关,市场份额较大的企业也都是采浆量排在前列的企业。
中国人血白蛋白市场份额(进口+国产)
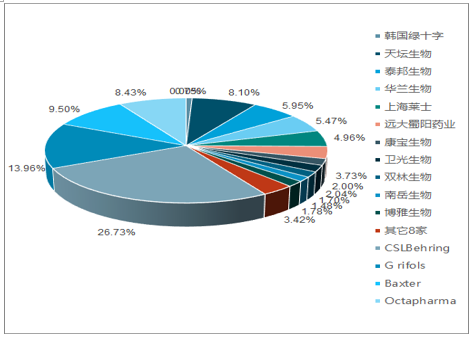
数据来源:公开资料整理
3、静丙供需缺口情况分析
静丙临床需求缺口大。一方面,我国静丙的使用量与发达国家差距较大。从 MRB的统计数据来看,2014 年我国人均静丙的使用量仅为世界主要发到国家平均水平的 1/6。另一方面,静丙的适应症在不断拓展,临床需求不断提高。静丙从最初用于原发性免疫缺陷逐渐扩展至自身免疫、免疫调节和抗感染治疗,同时静丙还可以广泛应用于 off label 的适应症乳格林-巴利综合征、川崎病、多发性硬化等。我国静丙市场的学术推广力度仍有待提高。
我国静丙的使用量与发达国家差距较大

数据来源:公开资料整理
我国静丙行业临床仍存在较大未被满足的需求,而供给端却受制于采浆量的增长,这导致近 10 年来,静丙价格呈现上升趋势。从 2008 年到 2018 年,规格为 5g/瓶的静丙,其年平均中标价格上涨了 89%;规格为 2.5g/瓶的静丙,其年平均中标价格上涨了 66%;规格为 1.25g/瓶的静丙,其年平均中标价格上涨了72%。
我国静丙每年平均中标价格变
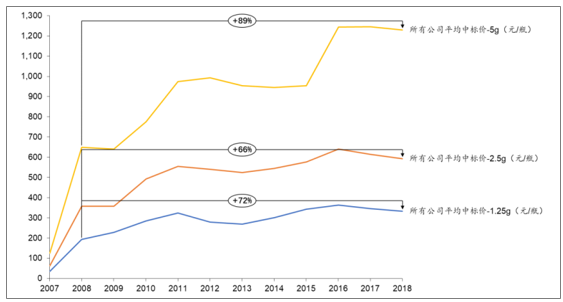
数据来源:公开资料整理
我国静注人免疫球蛋白历年批签发量变化
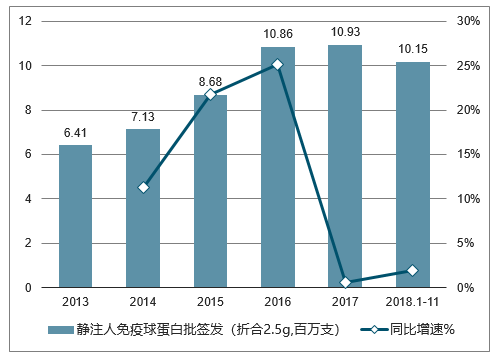
数据来源:公开资料整理
我国静脉注射人免疫球蛋白市场份额变化
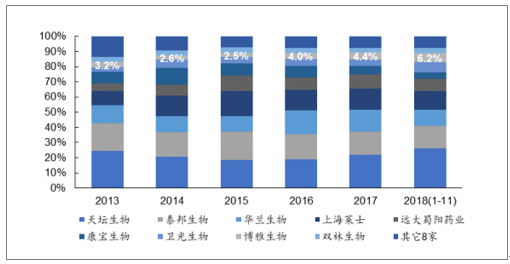
数据来源:公开资料整理
4、人凝血 VIII 因子
人凝血 VIII 因子的主要针对的患者人群是 A 型血友病患者。我国 A 型血友病患者目前治疗的比例仍很低。而且,与发达国家相比,我国人均凝血 VIII 因子的使用量远低于 WFH 推荐的标准。我国人凝血VIII 因子未来市场发展潜力巨大。目前我国人凝血 VIII 因子批签发量处于高速增长阶段。
我国人凝血 VIII 因子历年批签发量变化
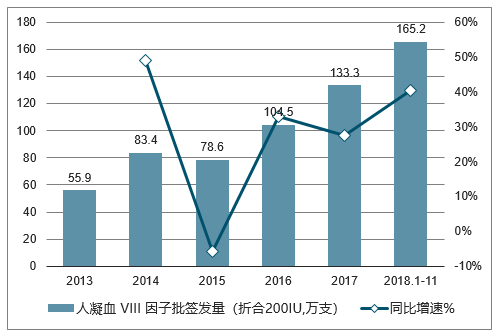
数据来源:公开资料整理
5、丹霞注入确定性较高
对于血制品企业来说,浆站资源和血浆综合利用率是核心竞争力。由于我国血制品行业监管较为严格,从 2001 年开始不再批准新的血制品生产企业,再加上这两年我国新浆站的批准速度放慢,外延并购成为血制品企业拓展血浆来源最快的途径。
中国 2018 年血制品行业主要公司浆站数量
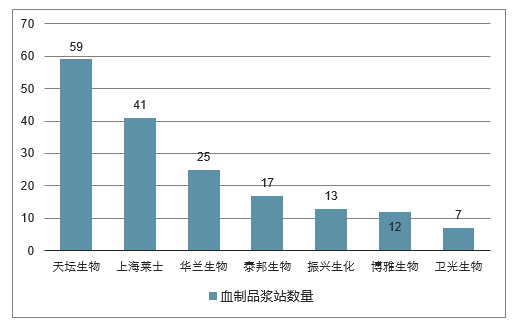
数据来源:公开资料整理
中国 2017 年血制品行业主要公司采浆量
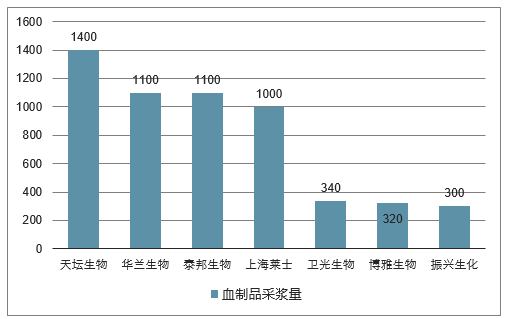
数据来源:公开资料整理
三、血液制品未来五大发展趋势
血液制品属于生物制品范畴,而且是一种特殊的药品,主要以健康人血浆为原料,是采用分离、纯化技术或生物工程技术以及多步血源性病毒灭活方法制备的有生物活性的制品。
(一)加大市场投入,加强临床医学推广
由于近期国家相继出台“药占比”“两票制”等系列政策,加上进口血液制品数量逐年增加和国内原料血浆采集量年均两位数的增长,市场供需矛盾正在发生改变。为了中国血液制品行业健康可持续发展,应积极整合国内血液制品生产厂家、科研院所、临床医院及检验机构等优势资源,以学术宣传和医学推广等模式,进一步教育、引导和培育血液制品市场,指导临床科室合理用药,挖掘血液制品临床适应证,千方百计将中国血液制品市场蛋糕做大,推动中国血液制品行业做大做强。
(二)建立行业监管长效机制,提升管理水平
针对国内目前血液制品行业法规滞后,单采血浆站标准严重缺失、信息化管理水平低下,无法保障全过程有效监控等问题。应尽快建立和完善相关法规标准,运用现代信息化技术和生物识别等智能化手段,建立全国单采血浆站与献血浆者信息化联网和不合格献血浆者数据库等,落实行业的有效监管,促进中国血液制品行业健康可持续发展。
(三)整合资源,推动行业并购提速
由于血浆来源受限,因此浆站数量多、采浆量大、血浆综合利用率高的企业具备明显的竞争优势,规模经济效益明显。目前我国血液制品行业集中度仍明显偏低,国内大型血液制品企业年投浆量一般为300~500吨,与国外血液制品巨头体量差距较大,企业间的兼并整合仍有很大空间。随着国家引导性政策不断出台以及行业自身的发展,近年来,我国血液制品企业之间的并购行为逐渐增多,行业集中度将会进一步提高。
(四)提高血浆综合利用率,开发新产品
为了充分合理地利用宝贵的血浆资源,各生产厂家应升级生产设备,提高生产工艺技术水平。积极采用新的蛋白分离纯化技术和方法,以提高产品的收率和纯度,推进原有产品和生产技术的升级换代,同时积极开展血浆蛋白的综合利用,大力研究开发新产品,并根据市场需要调整产品结构。另外鼓励和引导基因工程技术在血液制品生产中的应用,有重点地开展重组血浆蛋白的研制工作。
(五)积极开展国内外交流合作,引进先进技术和管理
创造条件和机会参加国际交流,有目标地进行技术引进。要建立信息网和数据库,对国际国内血液制品生产能力、水平、发展方向和路线有一个较为全面的资料、数据和信息的收集体系。投入资金和制定有利发展的政策,促进新技术的引进、使用和升级。对一些凝血因子类制品和微量蛋白成分的提取和纯化,选择合适的层析方法将显得尤为重要。
我国输血事业挑战与机遇并存
一百多年来,通过人类的不断摸索总结,输血医学取得了飞跃式发展,输血事业已纳入正规化和法制化的轨道,输血技术也在不断地发展、提高和完善。科学、合理、安全、有效的输血已成为全社会关注的焦点,我国输血事业既面临挑战,也将迎接机遇的到来。
一是,输血安全性将进一步提高。今后通过不断创新研究,提高血液制品中病毒检测方法的灵敏度,缩短窗口期,同时发展病原体灭活等技术,保证血液制品的安全。
二是,输血服务将更为完善。过去对于自身免疫性溶血性贫血患者的输血、RhD阴性孕产妇以及院前急救患者的紧急输血等问题一直存在争议,近年来随着越来越多对各种疑难输血问题的关注、探讨和研究,逐步规范化建立配合性输血、紧急输血流程,为临床输血提供更及时、优质的服务。
三是,输血的电子化信息管理。输血相关的资料通常要求保存十年之久,未来随着信息化管理的不断完善,这些大量、繁杂的数据将得到快速的分类管理、整合分析,从而大大提高临床输血工作效率和服务质量。
四是,输血新技术包括输血检验技术、血液制品检测技术、血液制备技术等以及新一代血液成分制品的应用研究将成为未来输血医学最有潜力的发展方向。
五是,作为目前最复杂的生物疗法,细胞治疗依然有许多的技术难点尚未突破,确切的作用机制还不清晰。细胞治疗伦理、细胞制品质量控制、肿瘤的CAR T和CAR NK细胞治疗、肿瘤的免疫检查点疗法、T细胞过继免疫治疗、干细胞移植治疗、基因编辑技术与干细胞的结合使用、基因修饰化细胞治疗、微囊化细胞移植治疗、3D打印在组织工程中的应用等,以及临床应用的有效性和安全性是目前关注和争论的焦点。
六是,临床输血是以关注患者转归为目的,以节约人类稀缺资源、保证临床安全有效输血为原则,充分利用各种成熟血液保护技术,多学科协作的用血全程管理。患者血液管理是临床用血管理的发展方向,在关注患者转归的前提下,追求患者治疗利益最大化。
七是,不断加强临床输血人才培养,学科技术的发展离不开人才,人才的培养离不开教育,因此培养输血技术相关人才梯队,对推动输血技术发展进步意义重大。
本站声明:网站内容来源于网络,如有侵权,请联系我们,我们将及时处理
